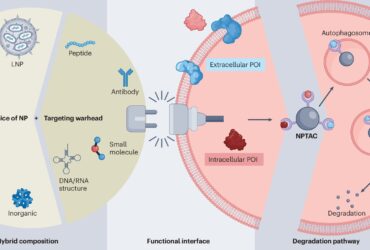
محققان کمپلکسهای زیستی ساختند که میتواند برای درمانهای هدفمند سرطان مورد استفاده قرار گیرد. این کمپلکسها، پروتئینهایی را هدف قرار میدهد که سلولهای سرطانی برای پنهان شدن از آنها استفاده میکنند.
هدف گرفتن پروتئینهایی که سلولهای سرطانی پشت آن قایم میشوند!
به تازگی دانشمندان در دانشگاه آبورن با همکاری محققانی از دانشگاه بازل در سوئیس، راه جدیدی برای پایدارتر کردن کمپلکسهای پروتئینی ارائه کردند که سرطان را هدف قرار میدهد. این یافتهها درها را به روی درمانهای بهتر و موثرتر سرطان باز میکند. این مطالعه به رهبری دکتر رافائل برناردی از دپارتمان فیزیک آبورن و دکتر مایکل نش از دپارتمان شیمی در دانشگاه بازل، انجام شده که در آن این گروه بر روی PD-L1، پروتئینی که تومورها از آن برای پنهان شدن از سیستم ایمنی استفاده میکنند، تمرکز دارند.
در بسیاری از سرطانها، PD-L1 به عنوان یک سپر عمل میکند، به سلولهای ایمنی متصل میشود و به آنها سیگنال میدهد که سرطان را نادیده بگیرند و به تومور اجازه میدهد تا بدون تشخیص رشد کند. با مسدود کردن PD-L1، مواد درمانی میتوانند به سیستم ایمنی کمک کنند تا سلولهای سرطانی را به طور مؤثرتری شناسایی کرده و به آنها حمله کند. در این مطالعه، محققان برهمکنشهای PD-L1 را با پروتئین کوچکی به نام Affibody بررسی کردند که برای چسبیدن به سلولهای سرطانی و کمک به حمل مستقیم داروهای ضدسرطان به تومور طراحی شده است.
این دو پروتئین با هم میتوانند ارائه درمانها را دقیقاً در جایی که نیاز دارند آسانتر کنند و درمانهای سرطان را مؤثرتر کنند و عوارض جانبی روی سلولهای سالم را کاهش دهند.
این مقاله که در ACS Nano منتشر شده است، مفهوم “ناهمسانگردی نیرو” را معرفی میکند، که نشان میدهد چگونه قدرت جفت شدن PD-L1 و Affibody بر اساس نقاط اتصال خاص متفاوت است. این تیم کشف کرد که تنظیم نقاط اتصال در PD-L1 میتواند این جفت را تا چهار برابر قوی تر کند.
دکتر دیگو گومز، محقق پسا دکترا در آبورن، گفت: «این پیشرفت میتواند نحوه اتصال داروها به پروتئینهایی مانند Affibodies را بهبود بخشد تا بتوانند سلولهای سرطانی را به طور مؤثر پیدا کرده و به آنها متصل شوند».
دکتر برناردی توضیح داد: «با تنظیم محل اتصال Affibodies، میتوانیم آنها را قوی تر کنیم تا مدت طولانی تری در بدن دست نخورده باقی بمانند و به آنها کمک کنیم تا به طور موثرتری به سلولهای سرطانی برسند.»
این تیم از آزمونهای آزمایشگاهی و مدلهای رایانهای برای سنجش اینکه چقدر این مجموعه پروتئینی میتواند کنار هم بماند، استفاده کردند. آنها دریافتند که با تنظیمات مناسب، این مجموعه نه تنها قوی میشود، بلکه حتی تحت تنش پایدارتر میشود، که آن را برای حمل مستقیم درمانها به سلولهای سرطانی ایدهآل میکند.
این کشف میتواند منجر به سیستمهای قابل اطمینانتر تحویل دارو شود و به محققان این امکان را میدهد تا درمانهای سرطانی را توسعه دهند که تومورها را با دقت بیشتری هدف قرار داده و مدت طولانیتری موثر باقی بماند. تیم دکتر برناردی اکنون به دنبال طراحی پروتئینهای Affibody قویتر است که میتواند انواع سرطانهای مختلف را با دقت بیشتری پیدا کرده و به آن بچسبد.
فراتر از تحویل دارو، این کار ممکن است به جراحی سرطان نیز کمک کند، جایی که Affibodies میتواند رنگهایی را حمل کند تا سلولهای سرطانی زیر نورهای خاص بدرخشند و به جراحان کمک کند تومورها را شناسایی و حذف کنند.