پیشرفت در پلتفورم فناوری تولید واکسنهای حاوی mRNA منجر به ساخت چندین واکسن ضدکرونا شده است. دانشمندان در حال توسعه فناوری ساخت واکسنهای mRNA برای محافظت در برابر بیماریهای دیگر مانند سرطان هستند. به تازگی یک واکسن RNA مبتنی بر هیدروژل توسعه یافته که طرح آن در قالب مقالهای در Nano Letters به چاپ رسیده است.

واکسنهای mRNA برای کووید ۱۹ موفقیتآمیز هستند، برای سرطان چطور؟
واکسنهای ضدسرطانی مبتنی بر RNA برای تولید آنتیژنهای مرتبط با تومور در سلولها با هدف تحریک سلولهای CD4+ و CD8+ برای از بین بردن یا کاهش ابعاد تومور طراحی شدهاند. موانع متعددی از جمله بیثباتی ذاتی و جذب کم سلولی mRNA برای دستیابی به موفقیت با واکسنهای RNA وجود دارد. فناوریهایی که میتوانند به محافظت از واکسنهای RNA در برابر تخریب و رساندن آنها به بافتهای هدف کمک کنند، برای پیشرفت این روشهای درمانی حیاتی هستند.
محققان سعی کردهاند از نانوذرات برای رساندن mRNA به بافتهای هدف استفاده کنند، اما آنها فقط برای یک تا دو روز پس از تزریق باقی میمانند که این زمان برای ایجاد پاسخ ایمنی کامل، کافی نیست. روش دیگر، استفاده از هیدروژل برای ترشح طولانی مدت است.
هر چند هیدروژل میتواند مشکل رهایش را حل کند، اما هنوز مسئله تخریب واکسن RNA قبل از ورود آن به سلولهای ارائهدهنده، آنتیژن وجود دارد. استفاده از افزودنیهای کمکی، مانند TLR، در واکسنهای RNA میتواند به تحریک سیستم ایمنی و شروع پاسخهای ایمنی ذاتی و سازگار کمک کند.
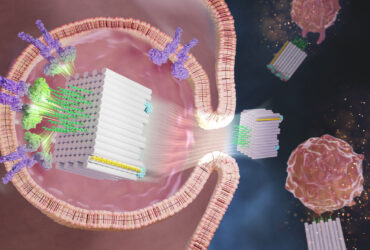
با استفاده از این راهبرد ترکیبی، محققان مرکز ملی علوم اعصاب و فناوری در چین، یک هیدروژل قابل تغییر ساختند که واکسن RNA و ماده کمکی برای ایمنیدرمانی سرطان را با خود حمل میکند. آنها در طراحی این سامانه جدید از اکسید گرافن استفاده کردند که سطح وسیعی دارد و این به معنی کارایی بالای بارگذاری دارو است.
محققان resiquimod (R848) را که یک آگونیست آبگریز TLR7 / 8 است بهعنوان افزودنی و اووالبومین کد کننده mRNA (mOVA) را بهعنوان واکسن mRNA مدل انتخاب کردند. mOVA به پلی اتیلنین با وزن مولکولی کم (LPEI) متصل شد. در نهایت، اکسید گرافن و LPEI با برهمکنش الکترواستاتیک مخلوط و ساخته شدند تا R848 و mOVA را در یک هیدروژل تزریقی کپسول کند.
محققان هنگام تأیید تشکیل نانوذرات درون هیدروژل، اعلام کردند که در محیط برونتنی رهایش ماده کمکی و واکسن RNA همانند هم انجام شده است و این نشان میدهد که آنها در نانوذرات با هم جمع شدهاند. علاوهبر این، محققان پایداری mOVA درون نانوذرات هیدروژل را بررسی کردند و دریافتند mOVA کپسوله شده حتی پس از ۱۰ روز در ژل پایدار است.
دادههای برونتنی نشان داد که نانوذرات هیدروژل توسط سلولها از طریق اندوسیتوز جذب شده است. بیان پروتئین اووالبومین در سلولهای ارائه دهنده آنتیژن با استفاده از وسترن بلات و الیزا تأیید شد.
رهاسازی طولانی مدت هیدروژل حاوی ماده کمکی و واکسن RNA با تزریق زیر جلدی در موش با هدف رساندن نانوذرات به غدد لنفاوی مورد بررسی قرار گرفت. محققان تأیید کردند که بخشی از mOVA حتی سی روز پس از تزریق هنوز در هیدروژل کپسول شده است.
بررسیها نشان میدهد که مقدار mOVA بهطور مداوم در طول ۳۰ روز کاهش یافته است. با تجزیه و تحلیل غدد لنفاوی پس از تزریق، این تیم تحقیقاتی تایید کرد که نانوذرات، با کمترین نشت به سایر اندامهای اصلی، به غدد لنفاوی منتقل میشوند.
در مدلهای موش مبتلا به ملانوم، محققان نشان دادند که نانوذرات هیدروژل حاوی واکسن RNA رشد تومور را مهار میکند. فرمول mOVA plus کمکی دارای بالاترین اثر درمانی است که به گفته محققان میتواند به دلیل عرضه بهتر آنتیژن، تحویل هدفمند به غدد لنفاوی و قابلیت آزادسازی طولانی مدت باشد.